Three-step biosynthesis of salicylic acid from benzoyl-CoA in plants
链接: 点击查看
关联仪器: B102 LC-MS液质联用系统,B102超高效液相色谱UPLC,B102飞行时间高分辨质谱仪SCIEX Triple TOF 5600
期刊名称: Nature
发表时间: 2025-07-23
提交用户: 刘亚楠
附件:
成果描述:
水杨酸(SA)是柳树皮中古老的消炎成分、药物阿司匹林的前体,更是植物对抗病原体的核心防御激素。其生物合成途径一直是植物科学领域的重大谜题。2025年7月23日,我院张跃林教授团队在国际顶尖期刊Nature发表题为“Three-step biosynthesis of salicylic acid from benzoyl-CoA in plants”的突破性研究,首次完整解析植物中一条全新的水杨酸合成通路“PAL/BSH途径”,并证明该通路在种子植物中广泛存在且高度保守。

植物合成SA主要依赖两条路径:异分支酸合成酶(ICS)途径和苯丙氨酸解氨酶(PAL)途径。以模式植物拟南芥为研究对象,ICS途径的合成机制已得到完整解析。近年来的证据表明,PAL途径在十字花科以外植物病原物诱导SA合成中同样扮演关键角色,但目前针对该途径的SA合成机制尚不清楚。尽管早期的研究利同位素标记的方法,发现苯甲酸(BA)是PAL途径的关键中间产物,但将BA转化为SA的苯甲酸2-羟化酶(BA2H)数十年来一直未被发现,成为领域内悬而未决的难题。
张跃林团队采用多学科攻坚策略,结合化学遗传筛选、转录组学、CRISPR基因编辑及精准代谢分析,在本氏烟草中成功捕捉到PAL途径的全貌。研究揭示了一条意想不到的三步酶促反应(图1):(1)酯化启动:苯甲酰辅酶A:苯甲醇苯甲酰转移酶(BEBT)催化苯甲酰辅酶A与苯甲醇结合,生成苯甲酸苄酯。(2)羟基化转化:苯甲酸苄酯氧化酶(BBO)对苯甲酸苄酯进行羟基化,生成水杨酸苄酯。(3)水解释放:水杨酸苄酯水解酶(BSH)裂解水杨酸苄酯,最终释放出水杨酸(SA)。
团队通过系统发育分析、跨物种互补实验(如水稻突变体验证)及病原体侵染测试证实,这条新发现的“PAL/BSH途径”在水稻、大豆等主要作物及柳树、杨树等多种种子植物中普遍存在且功能保守。该发现彻底颠覆了此前对PAL途径的初级假设,明确其在非十字花科植物中承担着SA合成的主要职责,解决了困扰学界数十年的关键问题。
此项研究不仅完善了植物抗病激素SA的生物合成版图,为解析不同植物类群(特别是主要粮食作物)的抗病机制差异提供了分子基础,更开辟了作物抗病育种的新方向。BEBT、BBO、BSH三个关键酶可作为抗病设计新靶点,通过基因编辑或调控其表达水平,精准增强作物的SA合成能力及抗病性。此外,该研究深化了对植物SA代谢的认识,有助于优化药用植物中水杨酸类活性成分的生产。
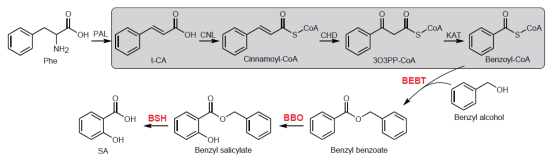
图1:新鉴定的植物中水杨酸(SA)生物合成途径模型
PALs将苯丙氨酸(Phe)转化为反式肉桂酸(t-CA),之后经过CNL、CHD和KAT参与的β-氧化途径(阴影标注)生成苯甲酰辅酶A(benzoyl-CoA)。BEBT催化苯甲酰辅酶A和苯甲醇(benzyl alcohol)发生酯化反应,生成苯甲酸苄酯(benzyl benzoate);苯甲酸苄酯经BBO催化发生羟基化,产生水杨酸苄酯(benzyl salicylate);最后, BSH裂解水杨酸苄酯,生成水杨酸(SA)。
 scu.edu.cn
scu.edu.cn